Galerias de Imagens > > Química Sintética
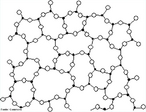
Grafite
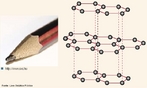
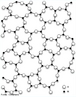
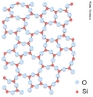
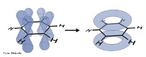
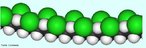
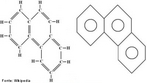
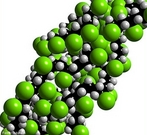
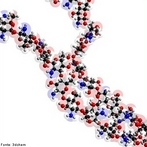
Representação da estrutura molecular da Grafite. A grafite é um dos alótropos do carbono; é um condutor, e pode ser usado, por exemplo, como os eletrodos de uma lâmpada elétrica de arco voltaico. A condutividade e outras características fisicas do grafite, como plano de clivagem e características lubrificantes se devem ao arranjo dos átomos no material, formando estruturas em forma de folhas, atraídas por ligações fracas(van der Walls). Nas "folhas", os átomos estão organizados como hexágonos, a semelhança dos favos numa colmeia, onde cada átomo de carbono ocupa um vértice. Como nesta estrutura cada carbono se liga a outros 3 átomos, "sobra" uma ligação para cada átomo. Estes elétrons formam uma grande ligação "deslocalizada" entre os átomos de carbono, semelhante a ligação metálica. A condutividade se dá ao longo da folha, de forma que no sólido, há variação da condutividade dependendo da posição em que este é medida ao longo do sólido (mais alta ao longo das folhas e menor perpendicularmente a estas. O acoplamento frouxo entre as folhas na grafite contribui a uma outra propriedade industrial importante, o pó da grafite é usado como um lubrificante seco. Os estudos recentes sugerem que um efeito chamado super lubrificação pode também esclarecer este efeito. A grafite é usada também dentro de lápis.
Palavras-chave: Grafite, carbono, alótropos, materiais.


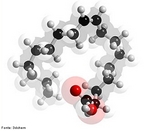
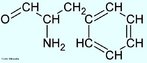



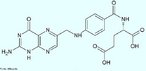
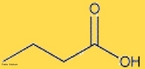

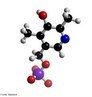
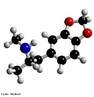
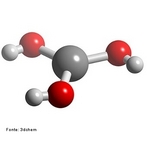
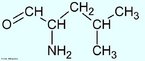
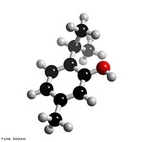
![Representação da molécula de Adrenalina ou epinefrina é um hormônio, derivado da modificação de um aminoácido aromático (tirosina), secretado pelas glândulas supra-renais, assim chamadas por estarem acima dos rins. Em momentos de "stress", as supra-renais secretam quantidades abundantes deste hormônio que prepara o organismo para grandes esforços físicos, estimula o coração, eleva a tensão arterial, relaxa certos músculos e contrai outros. Fórmula molecular C9H13NO3. Massa molar 183.204 g/mol. Nomenclatura IUPAC (sistemática) (R)-4-[1-hidroxi-2-(metilamino)etil]benzeno-1,2-diol <br/><br/> Palavras-chave: Adrenalina. Hormônios. Química orgânica. Doping.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_5_10adrenaline.jpg)
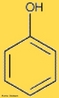
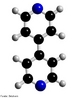
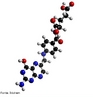
![Representação tridimensional da molécula de Adrenalina ou Epinefrina. A adrenalina é uma hormônio, derivado da modificação de um aminoácido aromático (tirosina), secretado pelas glândulas supra-renais. Em momentos de "stress", as supra-renais secretam quantidades abundantes deste hormônio que prepara o organismo para grandes esforços físicos, estimula o coração, eleva a tensão arterial, relaxa certos músculos e contrai outros. É chamada substância das emoções fortes. Nomenclatura IUPAC: 4-[1-hidroxi-2-(metilamino)etil]benzeno-1,2-diol. Fórumula molecular: C9H13NO3. Massa Molar: 183,204 g/mol. É utilizada também pela medicina em ressuscitações no caso de parada cardíaca ou para aumentar a duração de anestésicos locais devido ao seu efeito vasoconstrictor. <br/><br/> Palavras-chave: Moléculas. Adrenalina. Epinefrina. Substâncias químicas. Medicamentos. Drogas.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_6_1adrenaline_estruct.jpg)
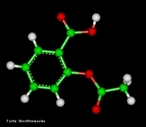
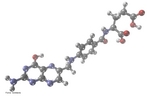
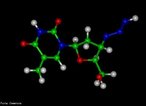
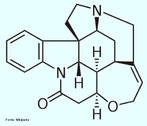
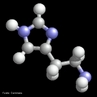
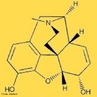
![Alcaloide encontrado na raiz de Rauwolfia serpentina, entre outras fontes vegetais. É um agente antiarrítmico da classe que aparentemente atua alterando a forma e o limiar dos potenciais de ação cardíacos. Nome IUPAC: (17R,21β)-ajmalan- 17,21-diol ou (1R,9R,10S,13R,14R,16S,18S)- 13-ethyl- 8-methyl- 8,15-diazahexacyclo [14.2.1.01,9.02,7.010,15.012,17] nonadeca- 2(7),3,5-triene- 14,18-diol Fórmula molecular: C20H26N2O2; Massa molar: 326.42 g mol-1 <br/><br/> Palavras-chave: Ajmalina. Alcaloides. Química orgânica. Toxicologia.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_7_1ajmalina.jpg)
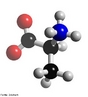
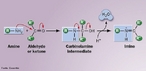

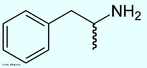
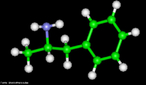
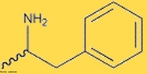
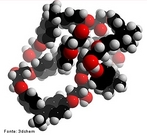

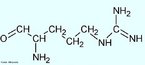
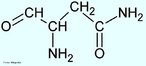
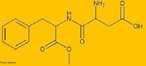
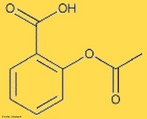
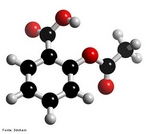
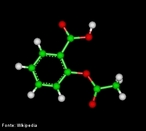
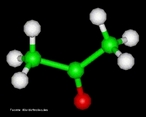
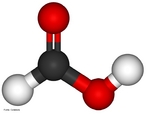
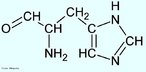
![Representação da molécula de atenolol, que é uma droga que pertence ao grupo dos beta bloqueadores, uma classe de drogas usadas principalmente em doenças cardiovasculares. Introduzida em 1976, o atenolol foi desenvolvido como um substituto para o propranolol no tratamento da hipertensão. Fórmula molecular C14H22N2O3. Massa molar 266,336 g/mol. Nomenclatura IUPAC (sistemática) (RS)-2-[4-[2-hidroxi-3-(1-metiletilamino)propoxy]fenil]etanamida. <br/><br/> Palavras-chave: Atenolol. Medicamentos. Química orgânica. Doping.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_12_9aatenolol.jpg)
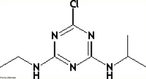


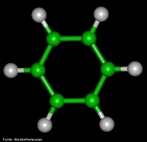
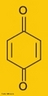
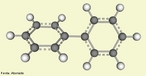

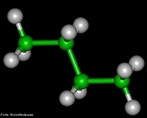
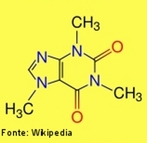
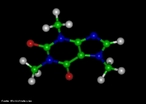
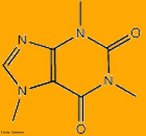

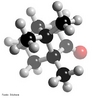
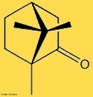


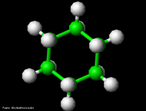
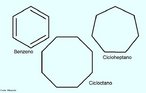
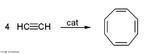
![Representação em 3D da molécula de cicloheptatrieno. Tropona ou 2,4,6-cicloheptatrieno-1-ona é um composto orgânico com alguma importância em química orgânica como um aromático não benzenóide (de estrutura derivada do benzeno).[2] O composto consiste de um anel de seis átomos de carbono com três grupos alquenos conjugados. O composto relacionado tropolona (2-hidroxi-2,4,6-cicloheptatrieno-1-ona) tem um grupo álcool (ou um enol incluindo a ligação dupla) próximo ao cetona. <br/><br/> Palavras-chave: Cicloheptatrieno. Molécula. Funções orgânicas.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_249cycloheptatriene.jpg)
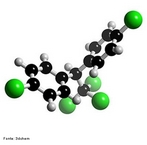
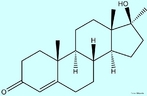
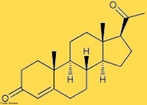
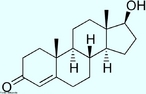
![Clostebol é um anabolizante que ajuda na cicatrização, ele não é utilizado para o aumento de massa muscular, porém um atleta que utilize uma pomada cicatrizante que contenha o Clostebol será flagrado no exame anti-doping. Fórmula molecular C19H27ClO2. Massa molar 322,869 g/mol. Nomenclatura IUPAC (sistemática) (8S,9S,10R,13S,14S,17S)-4-chloro-17-hydroxy-10,13-dimethyl- 1,2,6,7,8,9,11,12,14,15,16,17-dodecahydrocyclopenta[a]phenanthren-3-one <br/><br/> Palavras-chave: Clostebol. Medicamentos. Química orgânica. Doping.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_266clostebol.jpg)
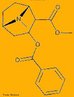
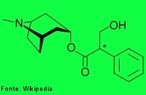
![Representação tridimensional da molécula de Cocaína ou benzoilmetilecgonina ou éster do ácido benzoico. É uma droga alcaloide, derivada do arbusto Erythroxylum coca Lamarck, estimulante com alto poder de causar dependência. Seu uso continuado, pode levar a dependência, hipertensão arterial e distúrbios psiquiátricos. A produção da droga é realizada através de extração, utilizando como solventes álcalis, ácido sulfúrico, querosene e outros. Nomenclatura IUPAC: 3-benzoiloxi-8-metil-8-azabiciclo. [3.2.1]octano-4-carboxilico. Fórmula Molecular: C17H21NO4. Massa Molar: 303,353 g/mol. <br/><br/> Palavras-chave: Moléculas. Cocaína. Substâncias químicas. Medicamentos. Drogas.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_272cocaine.jpg)
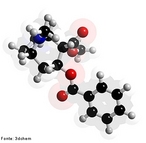
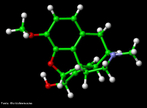
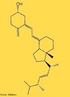
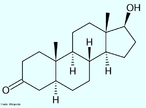
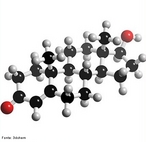
![Representação tridimensional da molécula de Colesterol, que é um esteroide lipídico encontrado nas membranas celulares e transportado no plasma sanguíneo de todos os animais. É um componente essencial das membranas celulares dos mamíferos. O colesterol tem um papel central em muitos processos bioquímicos, mas é mais conhecido pela associação existente entre doenças cardiovasculares e as diversas lipoproteínas que o transportam, e os altos níveis de colesterol no sangue (hipercolesterolemia). O colesterol é insolúvel em água e, consequentemente, insolúvel no sangue. Para ser transportado através da corrente sanguínea ele liga-se a diversos tipos de lipoproteínas, partículas esféricas que tem sua superfície exterior composta principalmente por proteínas hidrossolúveis. Existem vários tipos de lipoproteínas, e elas são classificadas de acordo com a sua densidade. As duas principais lipoproteínas usadas para diagnóstico dos níveis de colesterol são: * lipoproteínas de baixa densidade (Low Density Lipoproteins ou LDL): acredita-se que são a classe maléfica ao ser humano, por serem capazes de transportar o colesterol do fígado até as células de vários outros tecidos. Nos últimos anos, o termo (de certa forma impreciso) "colesterol ruim" ou "colesterol mau" tem sido usado para referir ao LDL que, de acordo com a hipótese de Rudolf Virchow, acredita-se ter ações danosas (formação de placas arteroscleróticas nos vasos sanguíneos). * lipoproteínas de alta densidade (High Density Lipoproteins ou HDL): acredita-se que são capazes de absorver os cristais de colesterol, que começam a ser depositados nas paredes arteriais (retardando o processo arterosclerótico). Tem sido usado o termo "colesterol bom" para referir ao HDL, que se acredita que tem ações benéficas. Nomenclatura IUPAC: (3β)-cholest-5-en-3-ol. Fórumula molecular: C27H46O. Massa molar: 386,65 g/mol. Nomenclatura sistêmica: 10,13-dimetil-17-(6-metilheptan-2-yl)-2,3,4,7,8,9,11,12,14,15,16,17-dodecahidro-1H-ciclopenta[a]phenanthren-3-ol Para a Associação Médica Americana, o nível desejável de colesterol LDL é menos do que 100 mg/dL (2,6 mmol/L), embora um novo alvo de <70 mg/dL pode ser considerado para indivíduos em alto risco baseado em alguns dos testes mencionados acima. O nível ideal de colesterol HDL é de >60 mg/dL. Uma proporção de colesterol total para o HDL outra forma útil de medição de menos de 5:1 acredita-se ser saudável. Como nota, os valores típicos de LDL para criança antes que os estágios iniciais de ateroma comecem a se desenvolver é 35 mg/dL. <br/><br/> Palavras-chave: Colesterol. Esteroide lipídico. Lipoproteínas. Funções químicas. Química orgânica.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_275cholesterol.jpg)
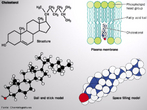



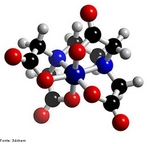
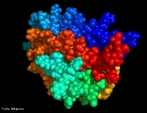

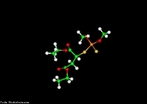
![Representação tridimensional da molécula de Estreptomicina. Foi o primeiro agente específico efetivo no tratamento da tuberculose. Foi também uns dos primeiros aminoglicosídeos descobertos. É um antibiótico bactericida de pequeno espectro. Foi descoberta pela equipe liderada pelo bioquímico norte-americano Selman Abraham Waksman, 19 de outubro de 1943, a partir da actinobacteria Streptomyces griseus, revelando-se um antibiótico relativamente inócuo para o homem, com excelentes resultados na luta contra a tuberculose quando combinado com a quimioterapia. A sua descoberta valeu a Waksman o Prêmio Nobel de Medicina, em 1952. Nomenclatura IUPAC:5-(2,4-diguanidino-3,5,6-trihydroxy-cyclohexoxy)- 4-[4,5-dihydroxy-6-(hydroxymethyl)-3-methylamino-tetrahydropyran-2-yl] oxy-3-hydroxy-2-methyl-tetrahydrofuran-3-carbaldehyde. Fórmula Molecular: C21H39N7O12. Massa Molar: 581,574 g/mol. <br/><br/> Palavras-chave: Moléculas. Estreptomicina. Substâncias químicas. Medicamentos. Drogas.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_394streptomycin.jpg)

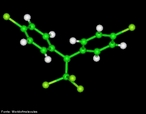
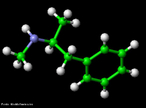
![Representação tridimensional da molécula de Fenfluramina. É uma droga que compunha a formulação de medicamentos anti-obesidade do grupo Fen-Fen (a outra droga era a Fentermina). É uma mistura racêmica de dois enantiômeros, dextrofluramina e levofenfluramina. Ele aumenta o nível do neurotransmissor de cerotonina, uma substância química que regula o humor, apetite e outras funções . Fórmula molecular C12H16F3N. Massa molar 231,257 g/mol. Nomenclatura IUPAC (sistemática) (RS)-N-ethyl-1-[3-(trifluoromethyl)phenyl]propan-2-amine <br/><br/> Palavras-chave: Fenfluramina. Medicamentos. Química orgânica. Doping.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_420fenfluramine3d.jpg)
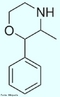
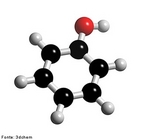
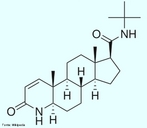
![Representação tridimensional da molécula de Fluoxetina. É um medicamento antidepressivo da classe dos inibidores seletivos da recaptação da serotonina. Suas principais indicações são para uso em depressão, transtorno obsessivo-compulsivo (TOC) e bulimia nervosa. É utilizado na forma de cloridrato de fluoxetina, como cápsulas ou em solução oral. Foi sintetizada e comercializada inicialmente pela companhia farmacêutica Eli Lilly com o nome Prozac®.Atualmente é comercializada no Brasil e em Portugal por vários laboratórios como medicamento genérico, estando sujeita a receita médica. A patente da Eli Lilly sob o Prozac expirou em Agosto de 2001,despertando um influxo de genéricos ao mercado. Só nos Estados Unidos, mais de 21,7 milhões de prescrições genéricas foram efectuadas em 2006, colocando-a na terceira posição entre os antidepressivos mais receitados, após a sertralina e o escitalopram. Nomenclatura IUPAC: (RS)-N-methyl-3-phenyl-3-[4- (trifluoromethyl)phenoxy]propan-1-amine. Fórmula Molecular: C17H18F3NO. Massa Molar: 309,3 g/mol (345,8 para HCl). <br/><br/> Palavras-chave: Moléculas. Fluoxetina. Prozac. Substâncias químicas. Medicamentos. Drogas.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_437prozac.jpg)
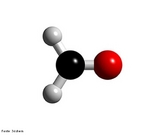
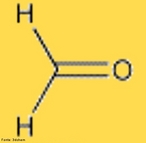

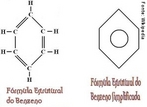
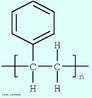

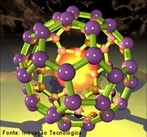
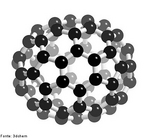
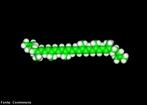
![Representação da estrutura molecular do Fulereno. Os fulerenos são a terceira forma mais estável do carbono, após o diamante e o grafite. Foram descobertos recentemente (1985), tornando-se populares entre os químicos, tanto pela sua beleza estrutural quanto pela sua versatilidade para a síntese de novos compostos químicos. Foram chamados de "buckminsterfullerene" em homenagem ao arquiteto R. Buckminster Fuller que inventou a estrutura do domo geodésico, devido à semelhança. Sua forma é de uma bola de futebol (domo geodésico) composta por 12 pentágonos e 20 hexágonos. Sua fórmula é C60. Os hexágonos mantém a planaridade (como no grafite que é plano por apresentar somente hexágonos) enquanto que cada pentágono inicia um ângulo de curvatura, sendo necessários 12 pentágonos para fechar a superfície sobre si mesma, formando uma bola. O fulereno C20 apresenta somente 12 pentágonos não possuindo hexágonos. O fulereno C70, que se parece a uma bola de rugby, tem mais hexágonos, porém com o mesmo número de pentágonos. Fulerenos são uma vasta família de nanomoléculas super aromáticas, altamente simétricas, compostas de dezenas de átomos de carbono sp2-hibridizados. Sua estrutura é em geral esférica, formada por hexágonos interligados por pentágonos, sendo estes últimos responsáveis pela curvatura da molécula e, consequentemente, por sua forma tridimensional [Kroto et al. 1985]. O representante mais conhecido da família dos fulerenos é o C60 (com 60 carbonos), um icosaedro truncado de simetria Ih, e um diâmetro de aproximadamente 1nm (namo-metro). Devido à sua forma tridimensional, suas ligações insaturadas e sua estrutura eletrônica, os fulerenos apresentam propriedades físicas e químicas únicas que podem ser exploradas em várias áreas da bioquímica e da medicina. Dentre a vasta gama de aplicações biomédicas dos fulerenos. <br/><br/> Palavras-chave: Fulereno. Carbono. Alótropos. Materiais.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_481fullerene_estruct_carb.jpg)
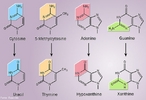
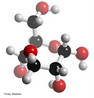
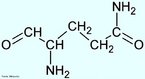


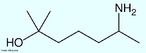
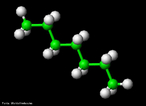
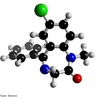
![A hidroclorotiazida é um diurético tiazídico usado principalmente na hipertensão arterial. A hidroclorotiazida pertence ao grupo dos saluréticos e atua no tubulo distal do nefron a nível do cotransportador sensível das tiazidas (TSC) que é um canal de suporte Na+/Cl-. Deste modo há uma maior excreção de NaCl e de água (por efeito osmótico). Esta perda de água aumenta a diurese e diminuí o volume líquido extracelular e consequentemente baixa a pressão sanguínea. Fórmula molecular C7H8N3ClO4S2. Massa molar 297,741 g/mol. Nomenclatura IUPAC (sistemática) 9-cloro-5,5-dioxo-5^6-tia-2,4-diazabiciclo[4.4.0]deca-6,8,10-triene-8-sulfonamida. Palavras-chave: Hidroclorotiazida. Medicamentos. Química orgânica. Doping.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_533hydrochlorothiazide.jpg)
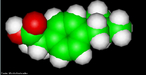

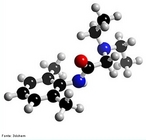
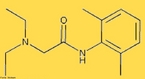



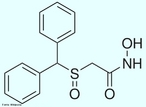
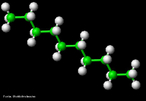
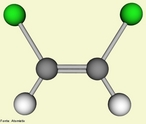
![O Modafinil é utilizado para tratar a depressão, esclerose múltipla e vários outros distúrbios associados à fadiga. Há relatos de que médicos estão sendo bombardeados por pessoas saudáveis solicitando receitas de modafinil como estimulante cognitivo que os faça dormir menos, trabalhar e se divertir mais. Fórmula molecular C15H15NO2S. Massa molar 273,35 g/mol. Nomenclatura IUPAC (sistemática) 2-[di(phenyl)methylsulfinyl]acetamide <br/><br/> Palavras-chave: Modafinil. Medicamentos. Química orgânica. Doping.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_682modafinil.jpg)

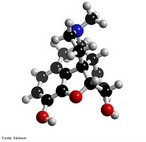
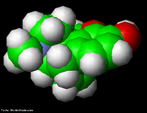

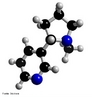
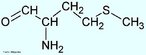
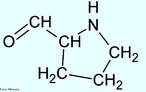
![Representação tridimensional da molécula de Nicotina. É uma substância alcaloide básica, líquida e de cor amarela, que constitui o princípio ativo do tabaco. Provoca cancro nos pulmões devido à metilização que ocorre no DNA (liga um radical metila, CH3). A pirrolidina (nicotina) sofre reações metabólicas (com NO+), oxidação e abertura do anel transformando-se em 4-(n-metil-n-nitrosamino)-1-(3-piridil)-1-butanona (CETONA) e 4-(n-metil-n-nitrosamino)-4-(3-piridil)-butanal (ALDEÍDO). O nitrosamino possui uma forma de ressonância onde um carbocátion é facilmente doado a uma base nitrogenada do DNA (guanina, citosina, adenina ou timina), causando uma falha de transcrição, levando à possibilidade de desenvolvimento do câncer. Nomenclatura IUPAC: 3-[(2S)-1-methylpyrrolidin-2-yl]pyridine. Fórmula Molecular: C10H14N2. Massa Molar: 162,26 g/mol. <br/><br/> Palavras-chave: Moléculas. Nicotina. Substâncias químicas. Drogas.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_717nicotine.jpg)
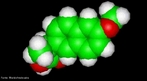
![Representação tridimensional da molécula de Nicotina é o nome de uma substância alcaloide básica, líquida e de cor amarela, que constitui o princípio ativo do tabaco. Provoca cancro nos pulmões devido à metilização que ocorre no DNA (liga um radical metila, CH3). A pirrolidina (nicotina) sofre reações metabólicas (com NO+), oxidação e abertura do anel transformando-se em 4-(n-metil-n-nitrosamino)-1-(3-piridil)-1-butanona (CETONA) e 4-(n-metil-n-nitrosamino)-4-(3-piridil)-butanal (ALDEÍDO). O nitrosamino possui uma forma de ressonância onde um carbocátion é facilmente doado a uma base nitrogenada do DNA (guanina, citosina, adenina ou timina), causando uma falha de transcrição, levando à possibilidade de desenvolvimento do câncer. Nomenclatura IUPAC: 3-[(2S)-1-methylpyrrolidin-2-yl]pyridine. Fórumula molecular: C10H14N2. Massa molar: 162,23 g/mol <br/><br/> Palavras-chave: Nicotina. Alcaloides. Drogas. Química orgânica.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_718nicotine.jpg)
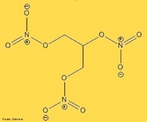














![Representação tridimensional da molécula de Rotenona, que é uma substância química inodora usada como inseticida, piscicida (causa morte de peixes) e pesticida. Ocorre naturalmente nas raízes e talos de várias plantas. Causa os sintomas do mal de Parkinson se injetada em ratos. Nomenclatura IUPAC: (2R,6aS,12aS)-1,2,6,6a,12,12a-hexahydro-2-isopropenyl-8,9-dimethoxychromeno[3,4-b]furo(2,3-h)chromen-6-one. Fórmula molecular: C23H22O6. Massa molar: 394,41 g/mol. <br/><br/> Palavras-chave: Rotedona. Química orgânica. Pesticidas. Inseticidas. Piscicida.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_877rotenone.jpg)

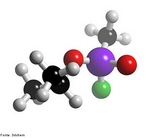
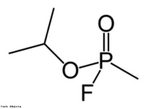
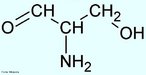

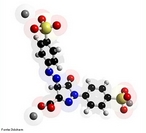


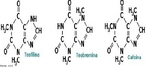
![Representação tridimensional da molécula de Tromantadina. Antiviral derivado da amantadina que tem atividade contra o vírus do herpes simples e o do herpes zóster. Indicado para infecções da pele e mucosas pelo vírus do herpes simples, principalmente na fase precoce e nas reinfecções. Eczema herpético. Manifestações dérmicas do herpes zoster. Nomenclatura IUPAC:N-1-adamantil-N-[2-(dimethylamino)ethoxy]acetamida Fórmula Molecular: C16H28N2O2. Massa Molar: 280,406 g/mol. <br/><br/> Palavras-chave: Moléculas. Tromantadina. Substâncias químicas. Medicamentos. Drogas.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_1004tromantadine.jpg)
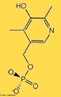
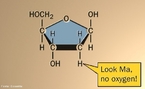
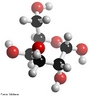
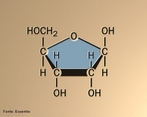
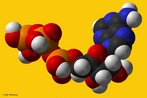
![A riboflavina (ou vitamina B2; antigamente designada também por vitamina G; nome sistemático 7,8-dimetil-10-ribitil-isoaloxazina[1]) é um composto orgânico (flavina) da classe das vitaminas. <br/><br/> Palavras-chave: Vitamina B2. Riboflavina. Vitamina G.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_1046vitaminb2.jpg)
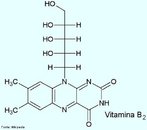
![A riboflavina (ou vitamina B2; antigamente designada também por vitamina G; nome sistemático 7,8-dimetil-10-ribitil-isoaloxazina[1]) é um composto orgânico (flavina) da classe das vitaminas.Molécula em 3D. <br/><br/> Palavras-chave: Vitamina B2. Riboflavina. Vitamina G.](http://www.quimica.seed.pr.gov.br/modules/galeria/uploads/5/thumb_1048vitaminb2.jpg)